
Макрокинетическая трансформация природных липидов для получения моторного топлива
ISSN 1812-3368. Вестник МГТУ им. Н.Э. Баумана. Сер. Естественные науки. 2017. № 5
99
где
t
— время реакции; TG
0
— начальная концентрация триглицеридов; DG
0
—
начальная максимальная концентрация диглицеридов; MG
0
— исходная кон-
центрация моноглицеридов.
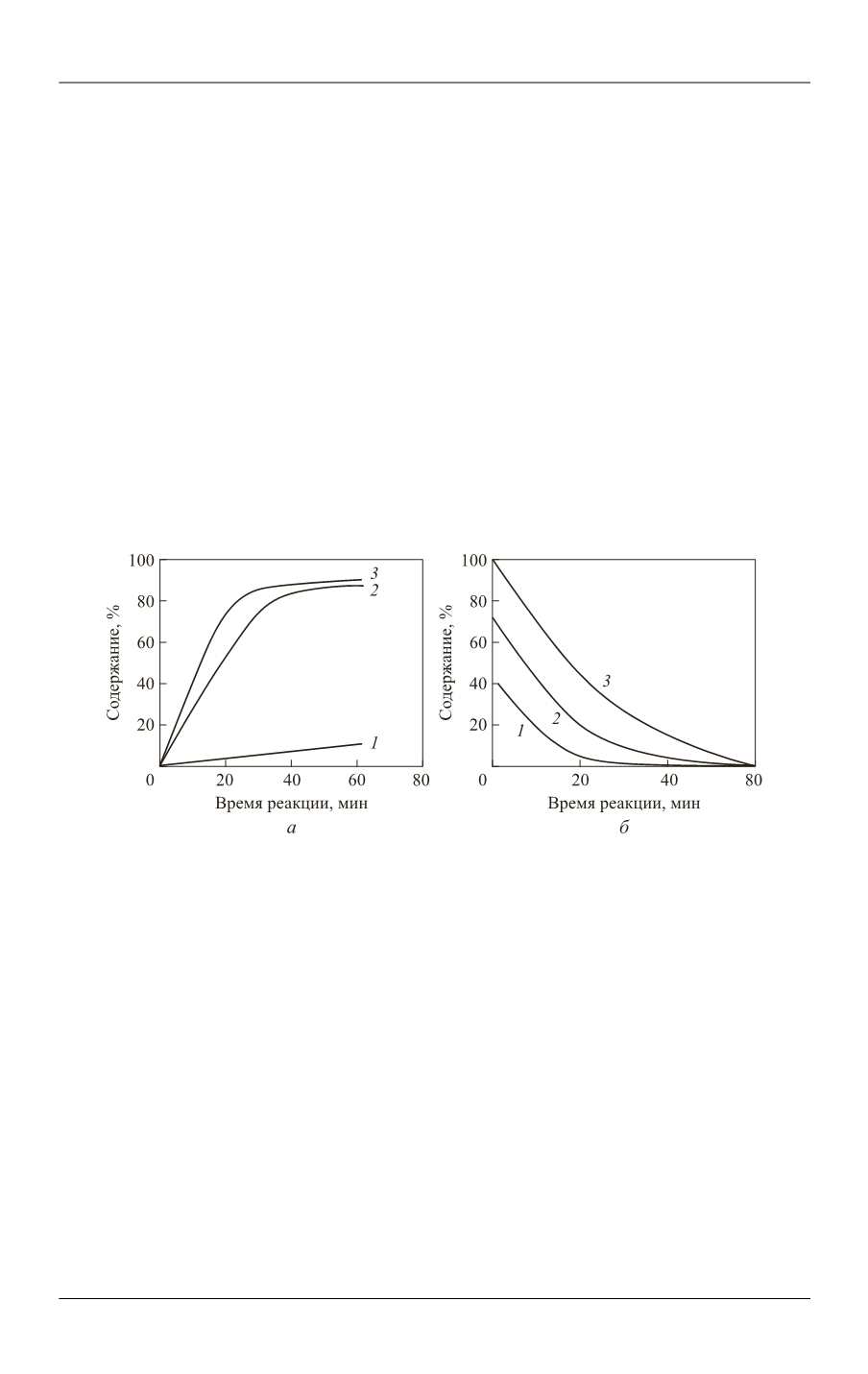
Типичные кинетические кривые процесса трансэтерификации приведены
на рис. 1. На начальной стадии реакции скорость образования этиловых эфиров
значительна, затем конверсия субстрата снижается и достигает стационарного
значения через 60 мин. Аналогичная зависимость наблюдается и при получении
метиловых эфиров. Можно предположить, что реакция трансэтерификации
является двухфазной. В первые 5–10 мин существуют фазы триглицеридов и
спирта, далее происходит гомогенизация системы с последующим формирова-
нием двухфазной системы вследствие образования избытка глицерина. Этот
эффект наблюдается визуально. Кривые накопления глицерина при этерифика-
ции метанолом и этанолом близки (рис. 1,
а
). Активность этанола в реакциях
трансэтерификации природных жирных кислот ниже, чем в случае использова-
ния метанола [20]. Применение этанола для проведения процесса этерификации
является оправданным ввиду токсичности метанола.
Рис. 1.
Типичные кинетические кривые процесса трансэтерификации:
а
— реакция трансэтерификации при температуре 70
С и 1,5 % KОН (
1
— глицерин;
2 —
этило-
вые эфиры;
3
— метиловые эфиры);
б
— образование продуктов реакции во время трансэтерифи-
кации животного жира этанолом при температуре 70
С и 1,5 % H
2
SO
4
(
1
— сырье с 40%-ным
содержанием моноглицеридов;
2
— жир с 70%-ным содержанием диглицеридов;
3
— триглице-
риды жира)
Полученные значения кинетических констант представлены в табл. 1. При
увеличении температурных режимов проведения реакции константа скорости
образования продукта
k
увеличивается в порядке
k
MG
>
k
DG
>
k
TG
. Этот подход
был использован для эмпирического определения энергии активации
E
.
Формализованная энергия активации процесса гидролиза три-, ди- и мо-
ноглицеридов в реакции трансэтерификации жиров составляла, кДж/моль:
ТG
DG — 55,6
DG
MG — 54,4
MG
GL — 23,2
















